¿Qué son las terapias térmicas y cuáles son sus efectos sobre las células
cancerígenas?
Dra. Citlalli Jessica Trujillo-Romero / Instituto Nacional de Rehabilitación-LGII
Dr. Texar Javier Ramírez Guzmán / Universidad Politécnica de Chiapas
M.C. José Raziel Sánchez Sánchez / Escuela Superior de Medicina - Instituto Politécnico Nacional
Dr. José de Jesús Agustín Flores Cuautle / Conahcyt-Tecnológico Nacional de México/Instituto Tecnológico de Orizaba
Dra. Raquel Martínez Valdez / Departamento de Ingeniería Biomédica / Centro de Ciencias de la Ingeniería / Universidad Autónoma de Aguascalientes
Resumen
Las terapias térmicas son tratamientos médicos que emplean frío o calor para el tratamiento de padecimientos presentes en el cuerpo humano. En oncología, se utilizan diferentes fuentes externas de calor para generar un incremento de temperatura en el tumor y producir diferentes efectos biológicos que provocan la muerte de las células cancerígenas. Estas fuentes de calor externas producen un incremento de temperatura en el cuerpo de manera regional o local, dependiendo del tamaño del tumor a tratar. Las terapias térmicas se clasifican de acuerdo con la temperatura alcanzada en la región de tratamiento o tumor, como: crioterapia, hipertermia y ablación térmica. La crioterapia consiste en lograr temperaturas por debajo de los - 20°C, temperatura a la cual se empiezan a formar cristales intracelulares que ocasionan la necrosis del tejido. Por otro lado, la hipertermia busca alcanzar temperaturas entre 41°C- 45°C en el tumor, ocasionando muerte celular dependiendo de la duración del tratamiento. Además, aumenta la efectividad de la quimioterapia y la radioterapia al sensibilizar las células cancerosas, aumentando el flujo sanguíneo en la región tratada, mejorando la entrega de oxígeno y medicamentos al tumor. En cambio, la ablación térmica produce muerte celular inmediata en el tumor al alcanzar temperaturas entre 60°C-100°C en segundos. Entre sus ventajas se encuentran que es mínimamente invasiva, requiere menor tiempo de recuperación, precisión y focalización de la inducción del calor, así como el hecho de que es un tratamiento localizado que minimiza el daño a tejidos sanos circundantes. Sin embargo, si no se tiene un control adecuado, se pueden causar quemaduras en tejidos sanos circundantes al tumor. Es necesario hacer notar que en este trabajo nos referiremos particularmente a las terapias basadas en el incremento de temperatura.
Introducción
Las terapias térmicas son tratamientos médicos que utilizan calor o frío para tratar diversas
afecciones y mejorar la salud general del cuerpo. Estas terapias se utilizan en diversas ramas de la
medicina, incluyendo la fisioterapia, la oncología y la rehabilitación. El calor generado por
diferentes fuentes externas es empleado para combatir diferentes tipos de cáncer. Estos tratamientos
aprovechan la sensibilidad que tienen las células cancerígenas al calor, lo que las hace más
vulnerables en comparación con las células sanas circundantes al tumor. Según la temperatura
alcanzada, las terapias térmicas enfocadas en el incremento de temperatura, se clasifican en
hipertermia (temperatura moderada) y ablación (temperatura elevada) [1]. Este trabajo se enfoca en
la descripción de las ventajas y desventajas de algunas terapias térmicas en aplicaciones
oncológicas. Además, se detallan los efectos que dichas terapias producen en las células
cancerígenas y sanas, de acuerdo con la temperatura alcanzada en la región de tratamiento.
Finalmente, se resaltan los efectos que favorecen el tratamiento efectivo de diferentes tipos de
cáncer.
Tipos de terapias térmicas más empleadas en tratamientos oncológicos:
Hipertermia
Consiste en alcanzar temperaturas entre 39 °C – 45 °C sobre el tumor, produce muerte celular (apoptosis) e incrementa la efectividad de la radioterapia y quimioterapia [2], esta se clasifica en:
- Hipertermia localizada: el calor se aplica directamente sobre la región del cuerpo en la que se encuentra el tumor. Las fuentes externas que generan el calor suelen ser las microondas, ondas de radiofrecuencia, el ultrasonido de alta intensidad y láseres. Esta terapia a menudo se utiliza en combinación con la radioterapia o quimioterapia para aumentar la efectividad de estos tratamientos [2][3].
- Hipertermia regional: el calor se dirige a una región más grande del cuerpo, como un órgano o una extremidad. Las técnicas de aplicación consisten en usar dispositivos especiales que envuelven la región a tratar. También, se utiliza la circulación de un medio líquido caliente encima de la región corporal bajo tratamiento. La hipertermia regional se utiliza para tratar cánceres localizados en una región específica del cuerpo y puede combinarse con otros tratamientos como la radioterapia y quimioterapia [3].
- Hipertermia corporal: se trata de calentar todo el cuerpo a temperaturas moderadas. El modo de aplicación consiste en el uso de cámaras especiales o baños de agua caliente con una temperatura controlada. Esta se utiliza, principalmente, para tratar cánceres metastásicos; es decir, cánceres que se han extendido a múltiples partes del cuerpo [3].
Beneficios de la Hipertermia Oncológica
Daño de las células tumorales: la hipertermia causa daño directo a las células cancerosas, induciendo
apoptosis o necrosis, dependiendo del tiempo de aplicación del tratamiento. La apoptosis es una de
las formas de muerte celular que es parte normal del desarrollo y mantenimiento de organismos
multicelulares comúnmente referida como muerte celular programada. Es un proceso fisiológico
necesario para eliminar células no deseadas o dañadas sin causar inflamación. Mientras que, la
necrosis es una forma de muerte celular que es resultado de una lesión aguda o daño severo, lo que
la convierte en un proceso patológico.
Sensibilización de las células tumorales: el calor provoca que las células cancerosas
incrementen su receptividad a la radioterapia y a ciertos tipos de quimioterapia, aumentando la
eficacia de estos tratamientos.
Mejora la circulación sanguínea: el calor aumenta el flujo sanguíneo del área tratada, lo
que puede mejorar la entrega de oxígeno y medicamentos al tumor.
Ablación térmica
Esta ocasiona muerte celular de manera inmediata (necrosis coagulativa) al lograr temperaturas muy altas (60 °C – 100 °C) sobre el tumor. Este método es especialmente útil para tratar tumores de dimensiones reducidas y ubicados en hueso, riñón, hígado, pulmones, entre otros órganos [4]. La ablación térmica puede ser una alternativa a considerar en pacientes no aptos a someterse a cirugía debido a problemas de salud, o porque el tumor está en una ubicación de difícil acceso. Existen diferentes técnicas para generar ablación térmica, entre las cuales se encuentran [5]:
- Ablación por Radiofrecuencia (RFA): utiliza ondas de radiofrecuencia para generar calor y destruir las células cancerosas. Se basa en introducir una aguja delgada a través de la piel y dirigirla al tumor, donde las ondas de radiofrecuencia generan calor focalizado, alcanzando temperaturas que destruyen el tejido tumoral.
- Ablación por Microondas (MWA): utiliza energía de microondas para calentar y destruir el tejido tumoral. De igual manera, se inserta una aguja sobre el tumor, y las microondas generan calor para destruir las células tumorales.
- Ablación por Láser: utiliza luz láser para incrementar la temperatura, destruyendo las células tumorales. El láser se dirige al tumor a través de una fibra óptica, generando el calor necesario para destruir el tejido canceroso. Esta técnica es menos utilizada, pero puede llegar a ser útil para tratar tumores cerebrales y de columna vertebral.
- Ablación por Ultrasonido Focalizado de Alta Intensidad (HIFU): utiliza ondas de sonido de alta frecuencia para aumentar la temperatura y destruir el tejido tumoral. Las ondas se enfocan en el tumor desde fuera del cuerpo, produciendo calor en el área objetivo sin necesidad de una incisión. Su uso es más común en tumores de próstata y útero.
Beneficios de la Ablación Térmica
Mínimamente invasiva: la ablación térmica generalmente se aplica de manera percutánea (a
través de la
piel), reduciendo el periodo de recuperación y la posibilidad de complicaciones en comparación con
una cirugía abierta para extirpar al tumor, por ejemplo.
Tiempos de recuperación cortos: debido a su aplicación percutánea los pacientes
suelen
recuperarse rápidamente.
Precisión y focalización: normalmente se utiliza una técnica de imagen, como el
ultrasonido
(US), la resonancia magnética (RM) o la tomografía computarizada (TC), para guiar el procedimiento,
y asegurar que el calor se aplique directamente sobre el tumor y no se causen daños al tejido sano
circundante.
Mayor eficacia al tratar tumores pequeños: presenta mayor eficacia y éxito en
tumores
pequeños y localizados, ya que se logra una destrucción completa del tumor.
Aunque la ablación térmica es más efectiva en el tratamiento de tumores pequeños, es
posible utilizar arreglos de agujas para tratar tumores de mayor tamaño [6]. Una de las principales
limitaciones para aplicar ablación térmica es la ubicación del tumor, ya que esta puede afectar la
viabilidad del procedimiento. En otras palabras, aplicar esta técnica a tumores cercanos a
estructuras vitales puede no ser adecuado, ya que se podrían producir daños no deseados en dichas
estructuras. Sin embargo, la ablación térmica es una opción terapéutica efectiva y menos invasiva
que la cirugía tradicional para el tratamiento de ciertas clases de cáncer, proporcionando
beneficios significativos para los pacientes.
Efectos de las terapias térmicas sobre las células cancerígenas
En las terapias térmicas existe una trasferencia de energía térmica al cuerpo humano a través de una fuente externa, que puede ser mediante microondas, radiofrecuencia, ultrasonido, o bien, láser. El incremento de temperatura del tejido produce efectos fisiológicos en los tejidos (Ver Figura 1) induciendo un cambio en su funcionamiento biológico (efecto biológico) [7].
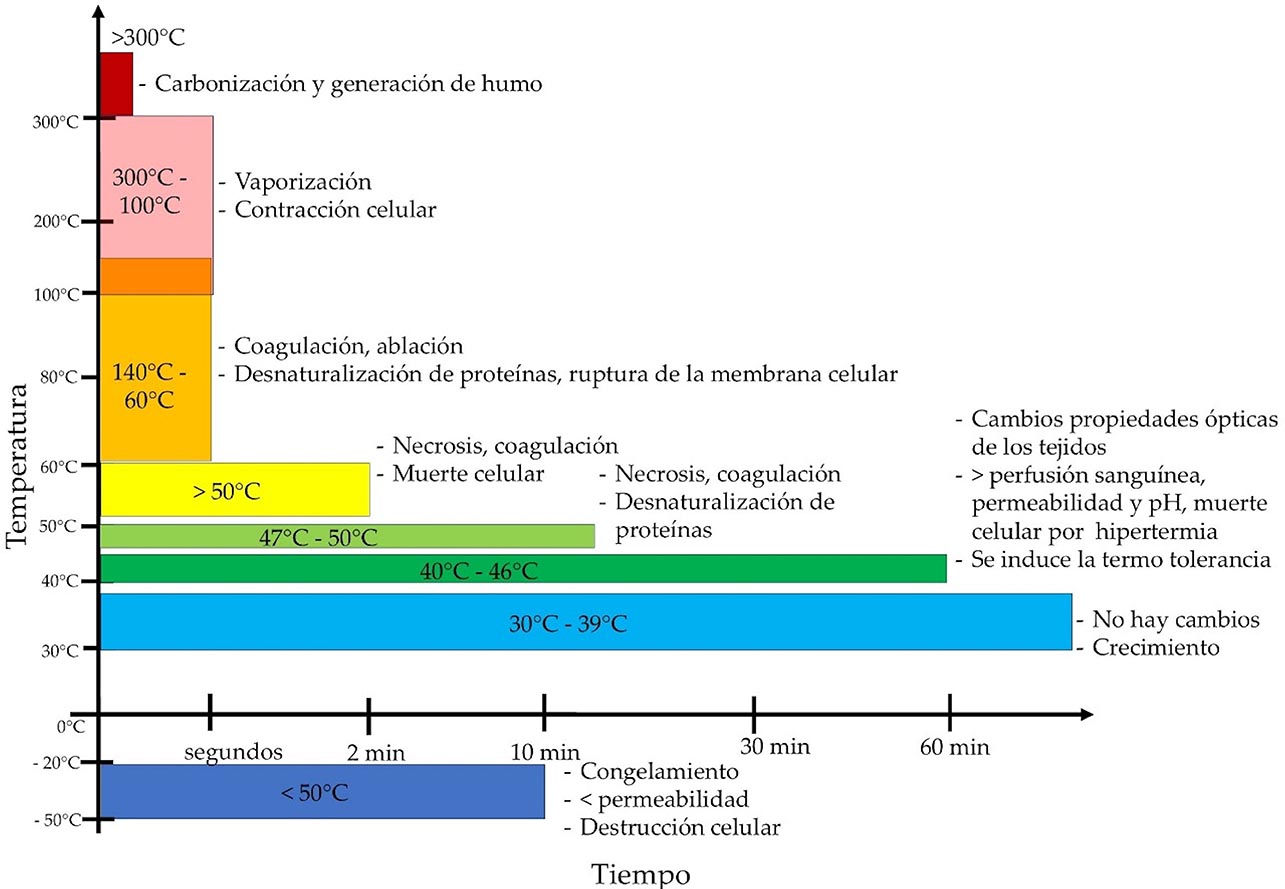
Figura 1. Efectos fisiológicos producidos en tejidos biológicos debido a un incremento de temperatura [8][9].
La efectividad de la termoterapia, específicamente de la hipertermia, se reduce conforme aumenta el
tiempo del tratamiento y el número de sesiones, esto se debe a la termotolerancia de las células; es
decir, a la resistencia al calor que desarrollan al ser expuestas a estas temperaturas durante
largos periodos [10][11], por esta razon es necesario estudiar la relación entre la fuente de calor,
el tumor, los tejidos sanos, y el efecto biológico producido, para incrementar la eficacia de la
terapia.
Muerte celular en función de la temperatura
La supervivencia celular es la capacidad de una célula para sobrevivir a lo largo del
tiempo, resistiendo diversas formas de estrés y daño que podrían conducir a su muerte. Temperaturas
mayores a 40 °C pueden inducir daño o muerte celular, dependiendo de la duración del tratamiento
[11]. Por otro lado, la tasa de crecimiento de las células aumenta en función del incremento de
temperatura; sin embargo, entre 40 °C y 41 °C esta se inhibe rápidamente [9], [11], siendo una parte
fundamental para el tratamiento de diversas variantes de tumores. En hipertermia, se produce un daño
irreversible en las células cancerígenas a temperaturas entre 42 °C – 45 °C aplicadas durante 30 min
- 60 min. Estas temperaturas son nocivas para las células, y las hacen más susceptibles a los
efectos dañinos de la radioterapia. El daño en las proteínas es el efecto molecular más relevante;
además, también se activa la muerte celular inducida por calentamiento [12]. Temperaturas superiores
a 50 °C (ablación térmica) pueden producir un daño celular irreversible dependiendo del tiempo de
aplicación. Temperaturas entre 100 °C – 300 °C producen vaporización; mientras que temperaturas
superiores a 200 °C, producen carbonización del tejido [8].
Condiciones del tumor
Los tumores presentan hipoxia (bajo nivel de oxigenación) debido a la reducción del flujo
sanguíneo. Tienen un pH ácido en comparación con los tejidos sanos, nutrición pobre y sensibilidad
al calor; además, su pH disminuye aún más durante la hipertermia, lo que beneficia la muerte
celular. Todas estas condiciones incrementan el daño térmico en el tumor [13]. Los tumores sólidos
presentan menor perfusión sanguínea comparada con la del tejido sano [14]. Es decir, la sangre
circula de manera más lenta a través de los vasos sanguíneos del tumor, suministrando menos oxígeno
y nutrientes esenciales, mientras la eliminación de productos de desecho disminuye. Esto ocurre
porque los vasos sanguíneos dentro del tumor están desorganizados y su flujo de sangre es irregular.
Por esta razón, los tumores son hipóxicos (presentan deficiencia de oxígeno), ácidos y resistentes a
la quimio y radioterapia [14]. Sin embargo, estas condiciones no afectan la acción de la
hipertermia; de hecho, se ha demostrado que se beneficia del estado hipóxico de las células [10].
Durante la hipertermia, el calor disipado debido al flujo sanguíneo es mayor en el tejido sano que
en el tumor; por lo tanto, el tumor alcanza temperaturas y daños mayores. Este incremento de
temperatura puede causar muerte celular mediante necrosis o apoptosis. En hipertermia (42.5 °C), la
muerte celular por apoptosis se ve promovida por la desnaturalización de las proteínas. Las
temperaturas menores a 42 °C generan niveles bajos de muerte celular; por lo tanto, para lograr
mayor efecto, los tiempos de tratamiento deben ser mayores a una hora [15]. A temperaturas mayores a
42 °C, la muerte celular incrementa significativamente; mientras que, a temperaturas de ablación
térmica (55 °C – 100 °C) predomina la muerte celular por necrosis [15]. La Figura 2 muestra los
efectos que se producen en el tejido sano y tumoral, así como en las células, al aplicarles
diferentes niveles de calor.
Termotolerancia
Se trata del incremento a la resistencia térmica que desarrollan las células como
consecuencia de tratamientos previos [11][16]. La termotolerancia es causada por las proteínas de
choque térmico que se producen en los tejidos expuestos a este [17]. Las proteínas de choque térmico
comprenden un conjunto de proteínas producidas como respuesta a condiciones de estrés, como el calor
extremo, la radiación ultravioleta, el frío, y otros factores que pueden causar daño celular. Estas
proteínas influyen de manera decisiva en la protección y reparación de las células dañadas. Por lo
tanto, la termotolerancia protege de la hipertermia, sobre todo a las células cancerígenas, ya que
las hace más resistentes al calor (menos sensibles a la hipertermia). Las células desarrollan
termotolerancia dependiendo de la intensidad del primer tratamiento de hipertermia; sin embargo,
este efecto solo dura unos cuantos días. Así, las sesiones de tratamiento se aplican con una
diferencia de tiempo mayor a 48 - 72 horas para lograr que la resistencia térmica que desarrollan
las células decaiga significativamente [16]. Mientras mayor es la temperatura alcanzada y el tiempo
de tratamiento, más letal es el efecto sobre el tumor y se reduce la termotolerancia inducida.
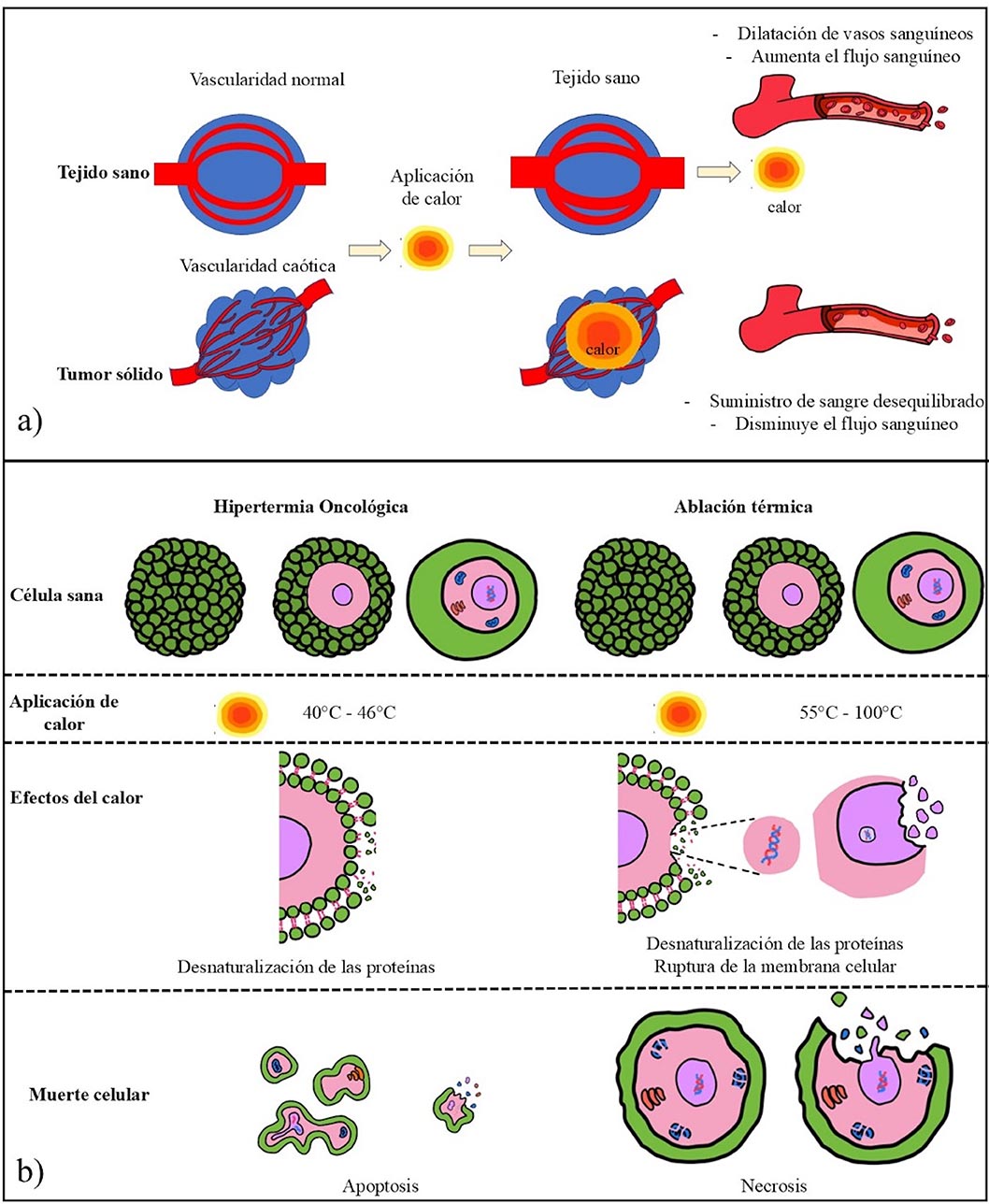
Figura 2. Efectos biológicos producidos por la aplicación de calor. a) Diferencias entren los efectos fisiológicos que se producen en tejido sano y tejido tumoral, b) efectos fisiológicos que se producen a nivel celular y conducen a la muerte celular [18]–[20].
Conclusión
Las condiciones específicas de los tumores pueden influir significativamente en la efectividad y los beneficios de las terapias térmicas como la hipertermia y la ablación térmica. Por lo tanto, estas terapias ofrecen beneficios significativos en el tratamiento del cáncer, especialmente cuando las condiciones del tumor son favorables para su aplicación. La evaluación cuidadosa de estas condiciones puede maximizar los resultados y proporcionar una opción terapéutica valiosa en el manejo del cáncer.
Financiamiento
Este trabajo fue financiado parcialmente por La Secretaria de Ciencia, Humanidades, Tecnología e Innovación (SECIHTI), fondo Ciencia de Frontera 2023 [Número de financiamiento: CF-2023-G-1010].
Referencias
[2] Q. Dai, B. Cao, S. Zhao, and A. Zhang, “Synergetic Thermal Therapy for Cancer: State-of-the-Art and the Future,” Bioengineering, vol. 9, no. 9, Sep. 2022. https://doi.org/10.3390/bioengineering9090474
[3] S. Jha, P. K. Sharma, and R. Malviya, “Hyperthermia: Role and Risk Factor for Cancer Treatment,” Achiev. Life Sci., vol. 10, no. 2, pp. 161–167, Dec. 2016. https://doi.org/10.1016/j.als.2016.11.004
[4] V. Lopresto, R. Pinto, L. Farina, and M. Cavagnaro, “Microwave thermal ablation: Effects of tissue properties variations on predictive models for treatment planning,” Med. Eng. Phys., vol. 46, pp. 63–70, 2017. https://doi.org/10.1016/j.medengphy.2017.06.008
[5] C. Brace, “Thermal Tumor Ablation in Clinical Use,” IEEE Pulse, vol. 2, no. 5, pp. 28–38, 2011. https://doi.org/10.1109/MPUL.2011.942603
[6] C. J. Trujillo-Romero et al., “Thermal Evaluation of Multi-Antenna Systems Proposed to Treat Bone Tumors: Finite Element Analysis,” Sensors, vol. 22, no. 19, p. 7604, Oct. 2022. https://doi.org/10.3390/s22197604
[7] WHO, “Electromagnetic fields and public health. Physical properties and effects on biological systems,” Fact Sheet, no. May, pp. 1-4 TS-Reference Manager DB p4 (via RIS-Export), 1998.
[8] R. W. Y. Habash, R. Bansal, D. Krewski, and H. T. Alhafid, “Thermal therapy, Part 1: An introduction to thermal therapy,” 2006. https://doi.org/10.1615/critrevbiomedeng.v34.i6.20
[9] J. R. Lepock, “How do cells respond to their thermal environment?,” Int. J. Hyperth., vol. 21, no. 8, pp. 681–687, 2005. https://doi.org/10.1080/02656730500307298
[10] G. Baronzio, G. Parmar, M. Ballerini, and A. Szasz, “A Brief Overview of Hyperthermia in Cancer Treatment,” J. Integr. Oncol., vol. 03, no. 01, 2014. http://dx.doi.org/10.4172/2329-6771.1000115
[11] J. R. Lepock, “Cellular effects of hyperthermia: relevance to the minimum dose for thermal damage,” INT. J. Hyperth., vol. 19, no. 3, pp. 252–266, 2003. https://doi.org/10.1080/0265673031000065042
[12] W. C. Dewey, “Arrhenius relationships from the molecule and cell to the clinic.,” Int. J. Hyperth., vol. 25, no. 1, pp. 3–20, Feb. 2009. https://doi.org/10.1080/02656730902747919
[13] P. Vaupel, F. Kallinowski, and P. Okunieff, “Blood Flow, Oxygen and Nutrient Supply, and Metabolic Microenvironment of Human Tumors: A Review,” Cancer Res., vol. 49, no. 23, 1989. [Online]. Available: https://aacrjournals.org/cancerres/article/49/23/6449/494447
[14] G. Baronzio, V. Cerreta, A. Baronzio, I. Freitas, M. Mapelli, and A. Gramaglia, “Thermo-Chemo-Radiotherapy Association: Biological Rationale, Preliminary Observations on Its Use on Malignant Brain Tumors,” 2013.
[15] P. B. Elming et al., “Hyperthermia: The optimal treatment to overcome radiation resistant hypoxia,” Cancers, vol. 11, no. 1. MDPI AG, 01-Jan-2019. https://doi.org/10.3390/cancers11010060
[16] A. Chicheł, J. Skowronek, M. Kubaszewska, and M. Kanikowski, “Hyperthermia - Description of a method and a review of clinical applications,” Reports Pract. Oncol. Radiother., vol. 12, no. 5, pp. 267–275, 2007. https://doi.org/10.1016/S1507-1367(10)60065-X
[17] H. H. Kampinga, “Cell biological effects of hyperthermia alone or combined with radiation or drugs: a short introduction to newcomers in the field.,” Int. J. Hyperth., vol. 22, no. 3, pp. 191–6, May 2006. https://doi.org/10.1080/02656730500532028
[18] K. M. Bruce, Fisiología - Edition 7 - By Bruce M. Koeppen, MD, PhD and Bruce A. Stanton, PhD Elsevier Inspection Copies, 7th ed. Elsevier.
[19] Robbins y Cotran, Patología estructural y funcional, 9.a ed. Elsevier, 2018.
[20] S. L. Cruz-Martín-del-Campo, C. González-Espinosa, A. K. Ruiz-Quiñonez, and C. J. Carranza-Aguilar, “Tipos de muerte celular y sus implicaciones clínicas,” El Resid., vol. 15, no. 3, pp. 97–112, 2020. https://dx.doi.org/10.35366/95960